アルギン酸による金属吸着
- アルギン酸水溶液中の金属イオン
- 吸着とは「気相または液相中の物質が、その相と接触するほかの相(液相または固相)との界面において、相の内部と異なる濃度で平衡に達する現象である」と定義されており、例えば、アルギン酸による金属吸着は、下図のように表わされる。
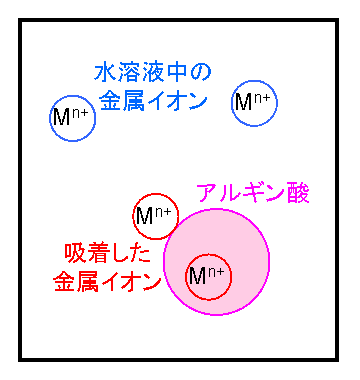
アルギン酸は、一価の金属イオンと結合して水溶性ゲルを、二価以上の金属イオンと結合して不溶性ゲルを形成することが知られている。水溶液中のゲルの表面や内部は水相とは異なる相であるとみなすと、上図のアルギン酸の表面や内部に結合した金属イオンはアルギン酸に吸着された状態である。
- アルギン酸の酸性官能基と金属イオンの相互作用
- アルギン酸が金属イオンを結合するのは、主に脱プロトン化したカルボキシル基(COO-)であることはアルギン酸の構成単糖であるb-D-マンヌロン酸とa-L-グルロン酸の化学構造から容易に推測される。
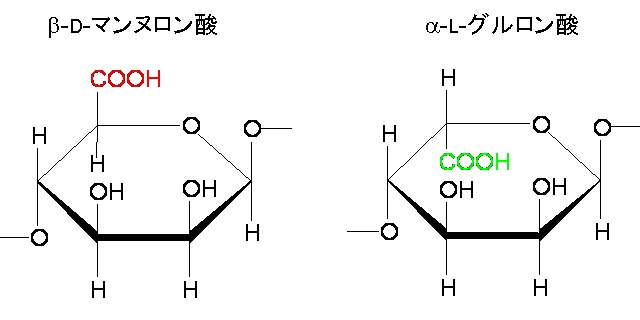
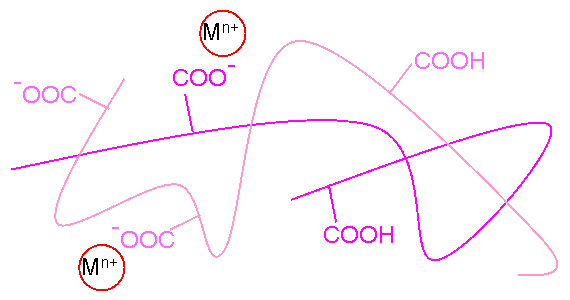
- アルギン酸の酸性および極性官能基と金属イオンの相互作用
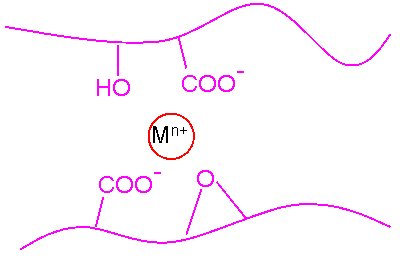
- 脱プロトン化したカルボキシル基と金属イオンが相互作用するだけではなく、極性官能基である水酸基(OH)やエーテル基(O)も金属イオンと相互作用する可能性がある。どの水酸基やエーテル基が金属イオンと相互作用するかは、アルギン酸の平均分子量や濃度、金属の種類、溶液の状態(pHや塩強度)などに依存する。
- エッグボックス構造
- コンブ中に含まれるアルギン酸は“エッグボックス構造”と呼ばれるa-L-グルロン酸が多く存在する部分構造を形成し、そのエッグボックス構造の比率が大きいと金属吸着能が高いことが知られている。
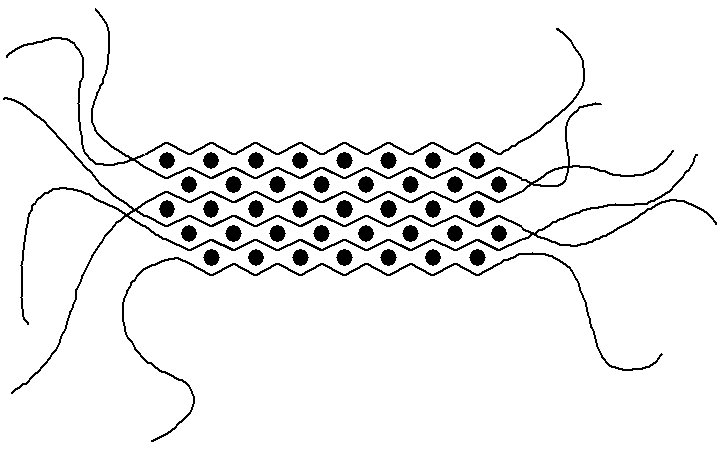
アルギン酸カルシウムのエッグボックス構造を化学構造から推測すると下図のように考えられる。
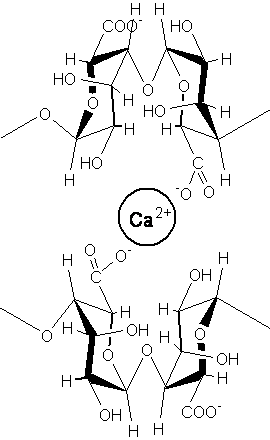
- アルギン酸カルシウムの立体構造モデル
- 密度汎関数計算によって推定された二つのa-L-グルロン酸の二量体モデルの立体構造が下図である。
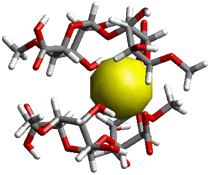
重要な点は、カルシウムイオンが鎖間(分子内あるいは分子間)を架橋するように結合していることである。アルギン酸がカルシウム塩になると不溶性沈殿を生じる実験事実から考えて、妥当なモデルである。
- アルギン酸金属錯体
- アルギン酸と結合する金属の錯形成能が高い場合には、アルギン酸の酸性および極性官能基を配位子として金属錯体が形成される。金属イオンのサイズやアルギン酸の状態(官能基の配向や距離など)によって、結合能に違いが生じる。錯形成能が高い金属であってもアルギン酸との吸着能が高いとは限らないので、アルギン酸の金属結合能を振動分光法、金属吸着能を原子吸光分光法によって解析し、両者の関係を調べることは有意義である。
研究概要にもどる






