赤外分光法による光合成膜蛋白質複合体の
構造と機能に関する研究
- 酸素発生型光合成
- シアノバクテリアや高等植物が営む<B>酸素発生型の光合成</B>は、地球の形成し大気環境を形成し、 高効率な酸素呼吸型生物の進化を可能にした。この枢要な反応は、葉緑体のチラコイド膜に含まれる光化学系IIで起こり、
その本質は4つのマンガンと1つのカルシウムにより形成されるMn4Caクラスターによる水の酸化反応であると考えられている。近年、好熱性シアノバクテリアを用いたX線結晶構造が報告され(図1)、構造の全貌が明らかになりつつある。しかしながら、Mn4Caクラスター近傍の構造、及び水の酸化反応機構に関しては詳細な解明には至っていない。
 図1.光化学系II酸素発生複合体(2量体構造、PDB2AXT)
図1.光化学系II酸素発生複合体(2量体構造、PDB2AXT)
光化学系II複合体(図2)はD1およびD2蛋白質から成るヘテロダイマーであり、集光性クロロフィル蛋白質から 光エネルギーを吸収した反応中心P680が電荷分離をおこし、矢印に沿って電子伝達が進行する。光照射により電子を放出してイオン化したP680は
チロシンを介して Mn4Caクラスターにより還元される。4回の光照射により4等量の酸化力を蓄積したMn4Caクラスター は2分子の水によって還元され、その副産物として1分子の酸素が発生する。
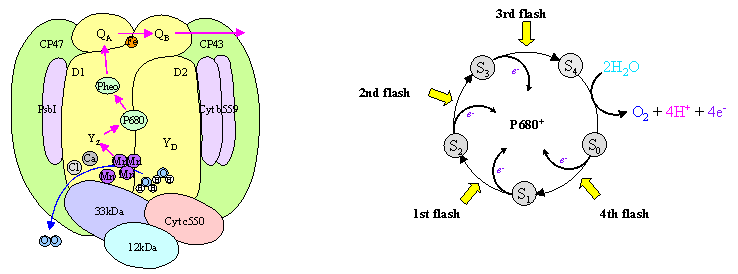
図2.光化学系II酸素発生複合体のモデル
図3.水の酸化反応サイクルのモデル
水の酸化反応機構は図3に示すKokサイクルに従って進行すると考えられている。Mn4CaクラスターにはS0からS4までの 5つの酸素発生反応中間状態がある。S0は最も還元された状態、S4は最も酸化された不安定な状態である。通常、暗順応状態である S1状態に光を照射すると電子を放出してS2状態に遷移する。さらなる光照射によりS3へと順次酸化 されていき、S4まで酸化された後に酸素を放出してS0状態にまで還元され、再びS1状態に戻ると考えられている。
- 赤外分光法による研究
- 赤外分光法は生体分子を非破壊的にモニタリングすることが可能であり、 特徴的な官能基由来の微小な構造変化の検出に優れた威力を発揮する。また、反応中間状態や反応に伴う構造変化の追跡など、
生体分子内で起こる反応機構を明らかにする上でも非常に有力な手法である。4000-1000cm-1の中赤外領域では 蛋白質を構成するポリペプチド、Mnに配位するアミノ酸配位子、基質水分子など、Mnクラスター周囲の情報を得ることができる。 一方、1000cm-1以下の低波数領域では、Mnクラスターの骨格振動や、基質水分子、アミノ酸配位子との相互作用など、 Mnクラスター自身についての情報が得られる。両者を組み合わせることにより、網羅的にMnクラスターの構造や水分解反応機構を検証することが
可能である。

図4.マンガンクラスターと周辺アミノ酸残基の配位構造モデル
- 図5にはS1→S2遷移に伴って起こる光化学系II酸素発生複合体の構造変化を赤外分光法により観測した例を示してある。光照射前後の赤外スペクトルを測定し、その差をとることにより図5のようなスペクトルが得られる。プラスのバンドはS2状態を、マイナスのバンドはS1状態の振動を反映している。1700-1500cm-1にはポリペプチド鎖のアミド結合に由来するアミドI、アミドIIの構造変化が現れている。1600-1300cm-1にはMnクラスターの配位子の可能性が高いカルボキシレートの伸縮振動が現れている。また、1100cm-1付近にはMnクラスターのヒスチジン配位子由来のバンドが出現している。さらに、3600cm-1付近にMnと相互作用する基質水分子の伸縮振動が現れると考えられている。このようにS状態間遷移の差を観測することにより、Mnクラスターや酸素発生反応機構を明らかにする上で非常に重要な情報を得ることが可能である。

図5.光化学系II酸素発生複合体の光誘起S2/S1赤外吸収差スペクトル
- 水の同位体置換よる研究
- 光合成酸素発生反応において基質となる水分子を同位体(H218O、D2O、D218O)
置換してS状態間赤外吸収差スペクトルを測定することにより、酸素発生反応過程において基質水分子が関与する振動モードの特定を行った。図6に
光化学系II酸素発生複合体の各S状態間赤外吸収差スペクトルとH218O置換の効果を示す。上から順にS1→S2、S2→S3、S3→S0、S0→S1遷移に対応した赤外吸収スペクトルである。黒いスペクトルは無置換、赤がH218Oで置換した試料のものである。ここでは水分子の酸素に関与する構造、化学種のみが同位体効果を示す。蛋白質やカルボキシレート配位子、ヒスチジン配位子由来のバンドにはほとんど効果が見られなかったが、Mnクラスターの骨格振動が出現する波数領域において顕著な効果が観測された。この領域には基質水分子が関与する振動モードが含まれている可能性があることから、さらに詳細に同位体効果を検証した。

図6.光化学系II酸素発生複合体の光誘起S状態間赤外吸収差スペクトルに及ぼすH218O置換の効果
- 図6と同様にD2O及びD218O置換試料を用いて同位体効果を調べた。図7に示すようにH216Oを用いたスペクトルとH218Oを用いたスペクトルの差(H216O/H218O)をとると酸素に関与する振動モードのみが検出される。 D216O/D218Oでも酸素に関与する振動モードが検出されるが、両者の共通のバンドはHなどを含まない酸素のみが関与する振動モードであると考えられる。それ以外のバンドは酸素と水素が関与する振動モードであると帰属できる。
- 次にH216O/D216OとH218O/D218Oの比較からは酸素などを含まない水素のみが関与する振動モードを特定することが可能である。それ以外は酸素と水素が関与する振動モードであると考えられる。このような手法でS状態間遷移で観測されたバンドの帰属を行った。結果を表1にしめす。

図7.水の同位体置換によるバンドの帰属

- 水分子由来の酸素のみが関与する振動モードとしてはマンガンクラスターの骨格振動や酸素分子形成過程の化学種などが考えられる。水素のみが関与する振動モードとしてはアミノ酸側鎖、蛋白質のペプチド結合に由来する構造が考えられる。また、酸素と水素の両者に関与する振動モードはOH間相互作用を含むものであり、Mnと基質水分子間相互作用に由来する酸素発生中間体の変化を反映している可能性がある。本研究ではすべてのS状態間遷移に伴うMnクラスターの構造変化を検出したこと、Mnクラスター骨格の酸素が水分子の酸素と置き換わっていることを明らかにした。光化学系II酸素発生複合体という超分子複合体中の特異的な構造変化だけを検出することができ、今回示した同位体置換の他にも、金属置換や部位特異的遺伝子変異などの手法を組み合わせることにより更なる詳細な情報を得ることが可能である。
-
光合成の研究テーマにもどる






